# 48 EFICACIA DE LOS ESQUEMAS DE PRIMERA LÍNEA PARA ERRADICACIÓN DE HELICOBACTER PYLORI SEGÚN EDAD: DATOS DEL REGISTRO LATINOAMERICANO (Hp-LATAMReg).
Reyes-Placencia D.¹, Corsi Sotelo O.², Quintana Martinic I.F.³, Soza Torres P.A.³, Remes-Troche J.M.⁴, Laudanno O.⁵, Otero W.⁶, Piscoya A.⁷, Varas Maire O.⁸, Otoya G.⁹, von Muhlenbrock C.¹⁰, Quera R.¹⁰, Castaño-Llano R. 11 , Ramírez García J.¹², Campos Núñez C.¹³, Portillo S.M.¹⁴, Cedrón H.15, Huidobro L.A.16, Hanna-Jairala I.17, Cabrera Hinojosa D.H.¹⁸, Acuña V.¹⁹, Jure Bustamante C.¹, Cantero D. 20 , Solano J. 20 , Romero M. 20 , Vargas-Alayza C. 21 , Araujo-Gil W. 21 , Barrios Fernández A. 22 , Mosca S. 23 , Moratorio I. 23 , Olano C. 23 , Parra Izquierdo V. 24 , Portillo-Miño J.D. 25 , Bolívar-Sáenz D.J. 26 , Tapia Valdivia C.G. 27 , Morales Inzunza M.A. 27 , Acuña Caroca D. 27 , Frías-Ordoñez J.S. 28 , Moreno Araya J.A. 13 , Saucedo R.E. 29 , Estay C. 30 , Madrid A.M. 30 , Simian D. 30 , Medel-Jara P. 1 , Uribe J. 1 , Pizarro Véliz M.¹, Latorre G.¹, Chahuan J.¹, Arenas A. 31 , Candia R.¹, Mansilla Vivar R. 32 , Vargas Domínguez J.I. 1 , Bosques Padilla F.J. 33 , Coss Adame E. 34 , Velarde Ruiz Velasco J.A.35, Higuera de la Tijera F. 36 , González Huezo M.S. 37 , Raña-Garibay R. 38 , Flores Rendón R. 39 , Gómez-Escudero O.40, Yamamoto Furusho J. 41 , Valdés Juárez E.I.⁴², Ortiz-Olvera N.X.43, Pizarro M.¹, Ahumaran G.⁴⁴, Rodríguez P.C.⁴⁵, Bedini O.A.⁴⁶, Ustares F.⁴⁷, Otero L.⁴⁸, Marulanda H.⁶, Otero E.⁴⁸, Trespalacios A.49, Cano-Català A.⁵⁰, Parra P. 51 , Nyssen O.P. 51 , Moreira L. 52 , Gisbert J.P. 51 , Riquelme A.¹. ¹ Departamento de Gastroenterología, Pontificia Universidad Católica de Chile, Santiago, Chile; ² Unidad de Endoscopia, Hospital de La Serena, La Serena, Chile; ³ Escuela de Medicina, Universidad Finis Terrae, Santiago, Chile; ⁴ Universidad Veracruzana, Veracruz, México; ⁵ Instituto Doctor Alfredo Lanari, Buenos Aires, Argentina; ⁶ Universidad Nacional de Colombia, Bogotá, Colombia; ⁷ Hospital Guillermo Kaelin de la Fuente, Lima, Perú; ⁸ Policlínico Varas Castrillo, Universidad Católica Boliviana, Tarija, Bolivia; ⁹ Hospital Nivel IV Guillermo Almenara Irigoyen, La Victoria, Lima, Perú; ¹⁰ Clínica Universidad de los Andes, Las Condes, Santiago, Chile; ¹¹ Clínica El Rosario, Medellín, Colombia; ¹² Clínica Liga contra el Cáncer, Lima, Perú; ¹³ Hospital Clínica Bíblica, San José, Costa Rica; ¹⁴ Centro de Enfermedades Digestivas, Hospital del Valle, San Pedro Sula, Honduras; ¹⁵ Clínica Anglo Americana, Lima, Perú; ¹⁶ Departamento de Ciencias Preclínicas, Facultad de Medicina, Universidad Católica del Maule, Talca, Chile; ¹⁷ Hospital Miguel H. Alcívar, Guayaquil, Ecuador; ¹⁸ Hospital Nacional Dos de Mayo, Lima, Perú; ¹⁹ Escuela de Medicina, Facultad de Medicina, Universidad de Chile, Santiago, Chile; ²⁰ Centro Médico La Costa, Grupo San Roque, Asunción, Paraguay; ²¹ E.S. II-1 Hospital de Chulucanas, Piura, Perú; ²² Centro Médico Las Torres S.A., Quetzaltenango, Guatemala; ²³ Hospital de Clínicas Dr. Manuel Quintela, Montevideo, Uruguay; ²⁴ Hospital Internacional de Colombia, Grupo de Inmunología Celular y Molecular (InMubo), Piedecuesta, Santander, Colombia; ²⁵ Grupo de Investigación en Infecciones y Cáncer (GINFYCA), Centro de Investigaciones Clínicas, Fundación Hospital San Pedro, Pasto, Nariño, Colombia; ²⁶ Gaster-Plaris, Instituto de Salud Digestiva, Red de Salud Colsubsidio, Bogotá, Colombia; ²⁷ Departamento de Medicina Familiar, Facultad de Medicina, Universidad Católica del Maule, Talca, Chile; ²⁸ Gastroenterología, Hospital Internacional de Colombia, Bucaramanga, Colombia; ²⁹ Hospital Regional Concepción, Concepción, Paraguay; ³⁰ Hospital Clínico Universidad de Chile, Santiago, Chile; ³¹ Clínica Alemana de Santiago S.A., Vitacura, Región Metropolitana, Chile; ³² Hospital Puerto Montt, Puerto Montt, Chile; ³³ Tecnológico de Monterrey, Monterrey, Nuevo León, México; ³⁴ Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán, Ciudad de México, México; ³⁵ Hospital Civil de Guadalajara, Guadalajara, Jalisco, México; ³⁶ Hospital General de México Dr. Eduardo Liceaga, Ciudad de México, México; ³⁷ Instituto de Seguridad Social del Estado de México y Municipios, Toluca, México; ³⁸ Hospital Español de México, Ciudad de México, México; ³⁹ ISSSTECALI, Tijuana, Baja California, México; ⁴⁰ Hospital Ángeles Puebla, Puebla, México; ⁴¹ Hospital Médica Sur, Ciudad de México, México; ⁴² Hospital Juárez de México, Ciudad de México, México; ⁴³ UMAE CMN Siglo XXI, IMSS, Ciudad de México, México; ⁴⁴ Clínica Monte Grande, Buenos Aires, Argentina; ⁴⁵ Instituto Modelo Córdoba, Córdoba, Argentina; ⁴⁶ Centro de Endoscopía Digestiva, Rosario, Argentina; ⁴⁷ Sanatorio Lavalle, Jujuy, Argentina; ⁴⁸ Centro de Gastroenterología y Endoscopía, Bogotá, Colombia; ⁴⁹ Pontificia Universidad Javeriana, Bogotá, Colombia; ⁵⁰ Fundació Institut de Recerca i Innovació en Ciències de la Vida i la Salut a la Catalunya Central, Vic, España; ⁵¹ Hospital Universitario de La Princesa, Instituto de Investigación Sanitaria Princesa (IIS-Princesa), Universidad Autónoma de Madrid (UAM), Centro de Investigación Biomédica en Red de Enfermedades Hepáticas y Digestivas (CIBERehd), Madrid, España; ⁵² Hospital Clínic de Barcelona, Centro de Investigación Biomédica en Red de Enfermedades Hepáticas y Digestivas (CIBERehd), Barcelona, Catalunya, España.Funding: Public policy “Strategies for Gastric Cancer Prevention in Chile” UC (AR); FONIS SA19/0188 (AR) «Cost-effectiveness of new population screening strategies for gastric cancer control in Chile»; FONDECYT 1230504 (AR) «Role of the genomic and microbiome profile in gastric carcinogenesis: prospective endoscopic follow-up»; ANID FONDAP 152220002 (AR) «CECAN: Centro para la prevención y el control del cáncer». and LEGACy “CeLac and European consortium for a personalized medicine approach to Gastric Cancer”; no 825832 of the Horizon 2020 programme of European Union (AR).
INTRODUCCIÓN: La infección por Helicobacter pylori (Hp) es altamente prevalente en Latinoamérica. Se ha planteado que la edad podría influir en la eficacia de la erradicación, aunque la evidencia regional es limitada.
OBJETIVOS: Evaluar la eficacia de los principales esquemas de primera línea sin probióticos para la erradicación de Hp, comparando pacientes menores de 60 años versus 60 años o más.
MÉTODOS: Estudio observacional prospectivo multicéntrico (2018-2025) que incluyó 3.854 pacientes de 12 países. Se analizaron tasas de erradicación por intención de tratar (ITT), ITT modificada (mITT) y por protocolo (PP) en los seis esquemas más utilizados.
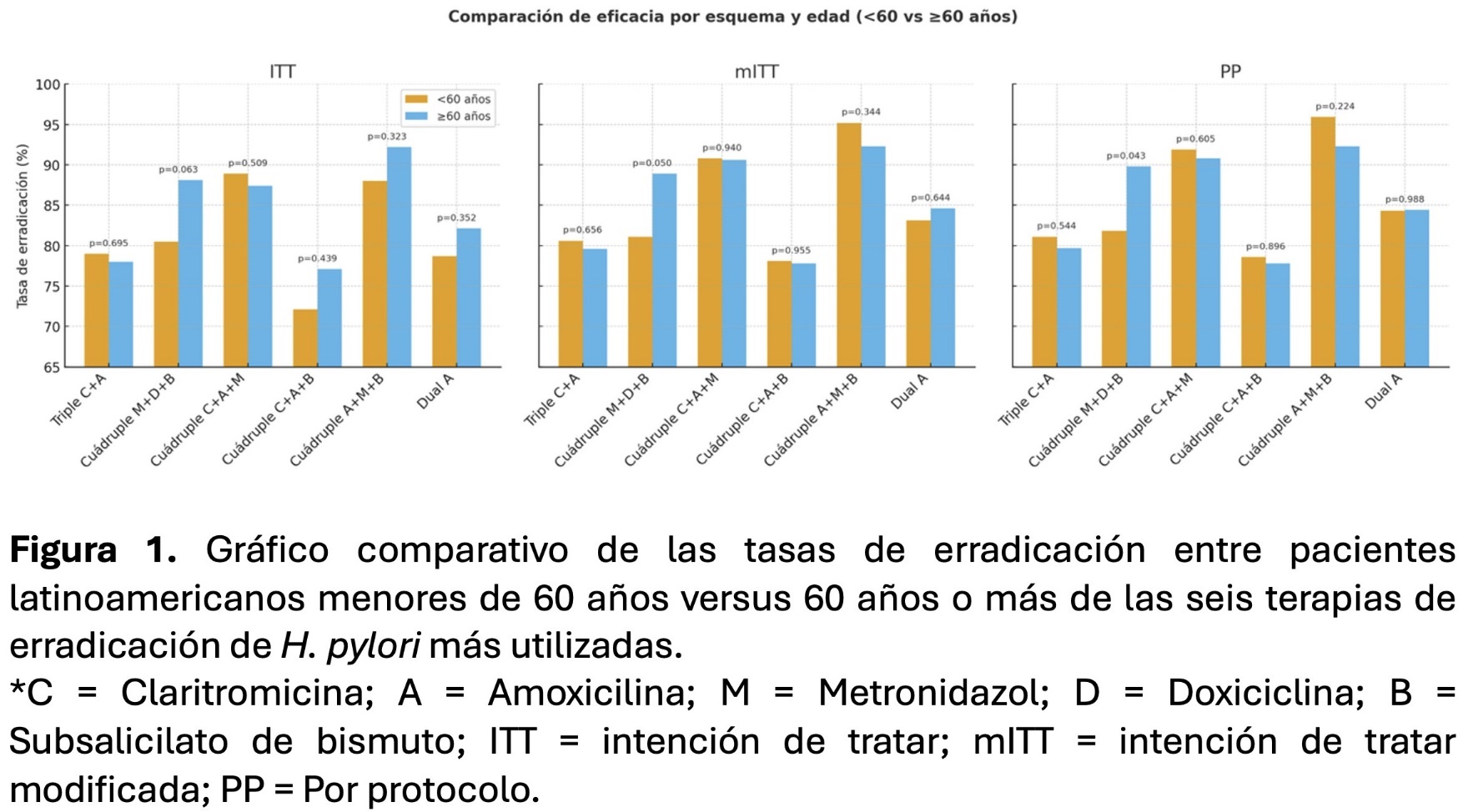
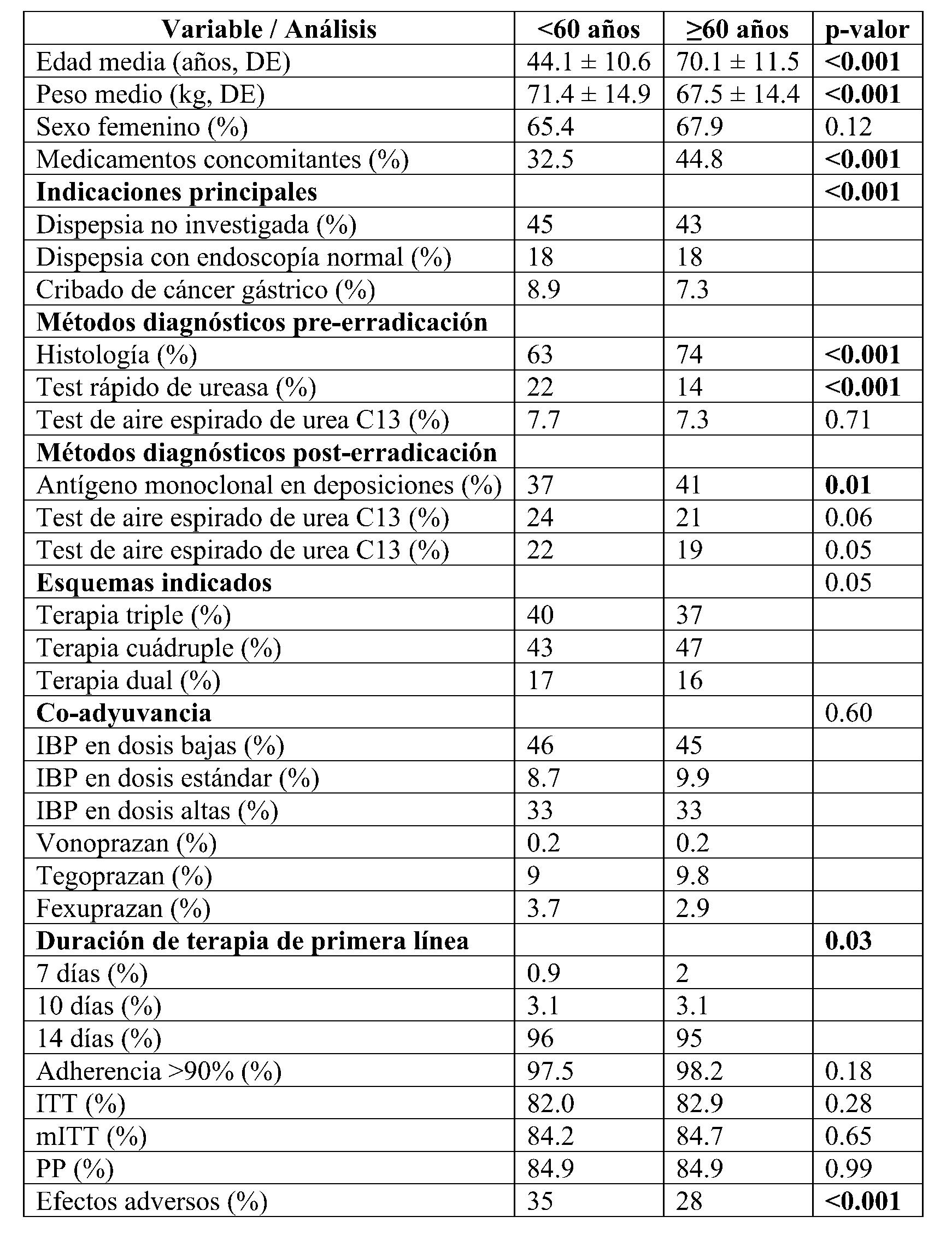
RESULTADOS: La edad media fue 44 (±10,6) años en <60 y 70 (±11,5) en >60 (p<0,001). Mujeres: 65% y 68% (p=0,12). La eficacia global fue: ITT 82% (<60) vs 83% (>60) (p=0,28); mITT 84% vs 85% (p=0,65); PP 85% en ambos (p=0,99). Los efectos adversos fueron más frecuentes en <60 (35%) que en >60 (28%) (p<0,001) (Tabla 1). La terapia triple mostró eficacia subóptima (~80%), al igual que la dual (<85%), mientras que las terapias cuádruples concomitante y con bismuto alcanzaron tasas cercanas al 90%, sin diferencias significativas por edad (Figura 1).
CONCLUSIÓN: En Latinoamérica, la eficacia de la erradicación de Hp es similar entre <60 y >60 años, aunque los pacientes mayores reportan menos efectos adversos. Las terapias triples y duales continúan siendo insuficientes, consolidándose las cuádruples con o sin bismuto como esquemas de primera línea óptimos.